「禁忌を含む注意事項等情報」等については
電子添文をご参照ください。
- 試験デザイン:
- 第Ⅱ相、無作為化、ダブルクロスオーバー、非盲検、実薬対照
- 対象患者:
- 以下の①②を満たした18歳以上60歳以下のPKU患者24例
- ①過去に少なくとも1回、血中Phe濃度が360µmol/L以上を記録
- ②スクリーニング期間のいずれかの時点で血中Phe濃度が450µmol/L以上
又は直近3回の血中Phe濃度測定値(スクリーニング時を含む)の平均が450µmol/L以上
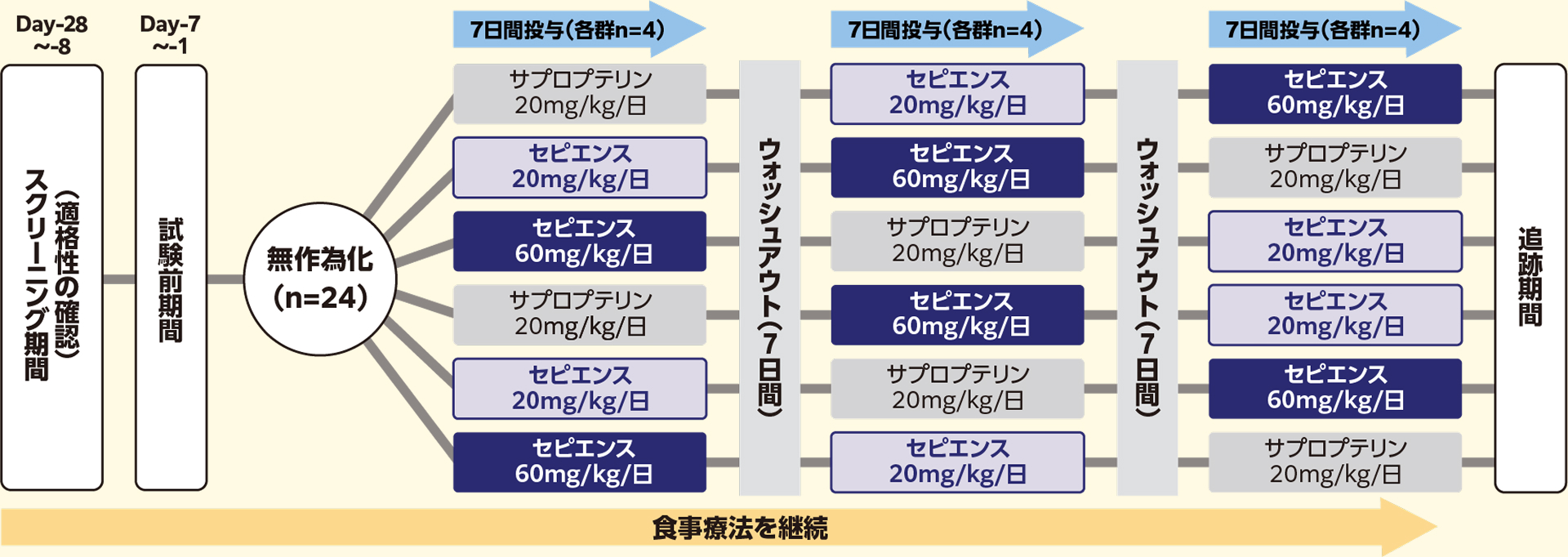
サプロプテリンを使用していた患者は、試験前期間の開始24時間前にサプロプテリンを中止
主要評価項目
血中Phe濃度のベースラインからの平均変化量
副次評価項目
- ・血中Phe濃度のベースラインからの経時的な平均変化量
- ・治験薬投与下で発現した有害事象(TEAE)の重症度及び発現頻度など
血中Phe濃度の解析
- 週平均解析:
- 各投与期間のDay3、5、7の血中Phe濃度の平均値をDay1投与前の血中Phe濃度と比較
- ランドマーク解析:
- 各投与期間のDay7の血中Phe濃度をDay1投与前の血中Phe濃度と比較
追跡期間
- 最終投与後48時間以内:
- 来院による安全性及びPhe評価
- 最終投与から7~10日後及び28~32日後:
- 電話による有害事象の確認
データベースロック日:

