有効性
主要評価項目
血中Phe濃度のベースライン*1からの平均変化量
血中Phe濃度の平均変化量は、セピエンス60mg/kg群の週平均解析で-206.4µmol/L、ランドマーク解析で-240.9µmol/Lでした。
週平均解析
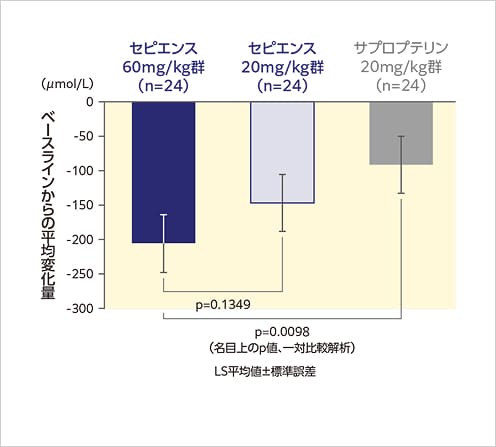
ランドマーク解析
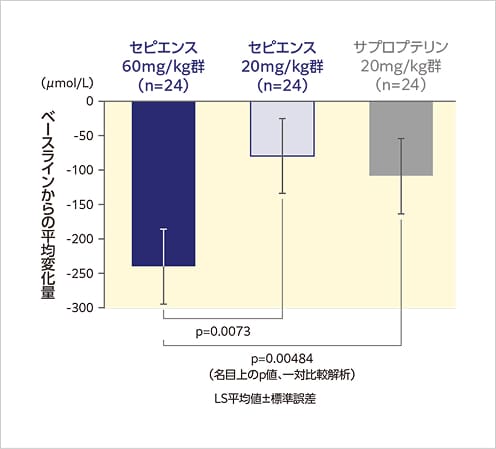
【ベースライン時の血中Phe濃度(µmol/L、平均値)】セピエンス60mg/kg群:727.8、セピエンス20mg/kg群:694.2、サプロプテリン20mg/kg群:710.4
副次評価項目
古典的PKU患者における血中Phe濃度のベースライン*1からの平均変化量
古典的PKU患者において、血中Phe濃度の平均変化量は、セピエンス60mg/kg群の週平均解析で-150.8µmol/L、ランドマーク解析で-114.9µmol/Lでした。
週平均解析
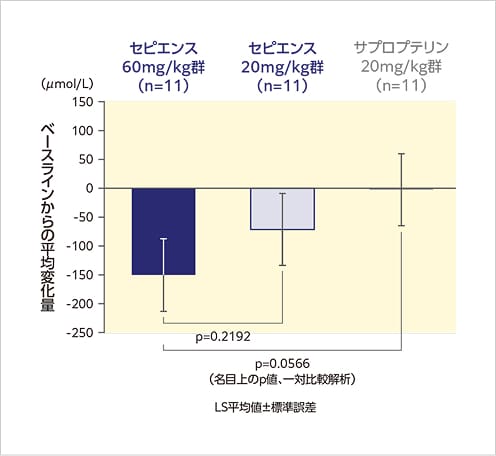
ランドマーク解析
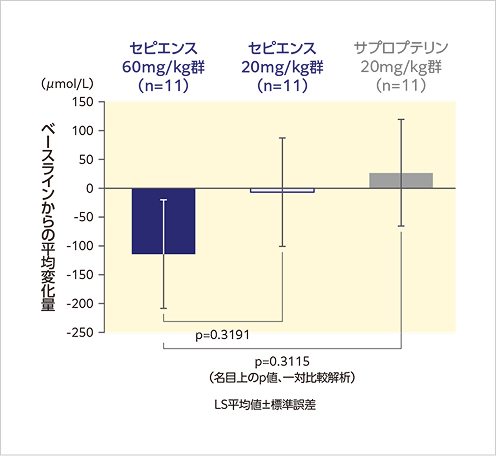
【ベースライン時の血中Phe濃度(µmol/L、平均値)】セピエンス60mg/kg群:947.2、セピエンス20mg/kg群:944.6、サプロプテリン20mg/kg群:903.5

