「禁忌を含む注意事項等情報」等については
電子添文をご参照ください。
- 試験デザイン:
- 第Ⅲ相、多施設共同、2パート、無作為化、二重盲検、プラセボ対照
- 対象患者:
- 以下の①~③に該当するすべての年齢のPKU患者157例
- ①過去に少なくとも2回血中Phe濃度が600µmol/L以上を記録
- ②スクリーニング期間中のいずれかの時点で血中Phe濃度が360µmol/L以上
- ③直近3回の血中Phe濃度測定値(スクリーニング時を含む)の平均が360µmol/L以上
当サイトはセピエンスを適正にご使用いただくための情報を提供しております。
「禁忌を含む注意事項等情報」等については
電子添文をご参照ください。

フェニルケトン尿症(PKU)患者を対象に、セピエンスを経口投与したときの有効性と安全性を評価する。
高フェニルアラニン(Phe)血症を伴うPKUと診断され、本試験中にPhe制限食を継続する意思がある患者(パート1:157例、パート2:110例)。
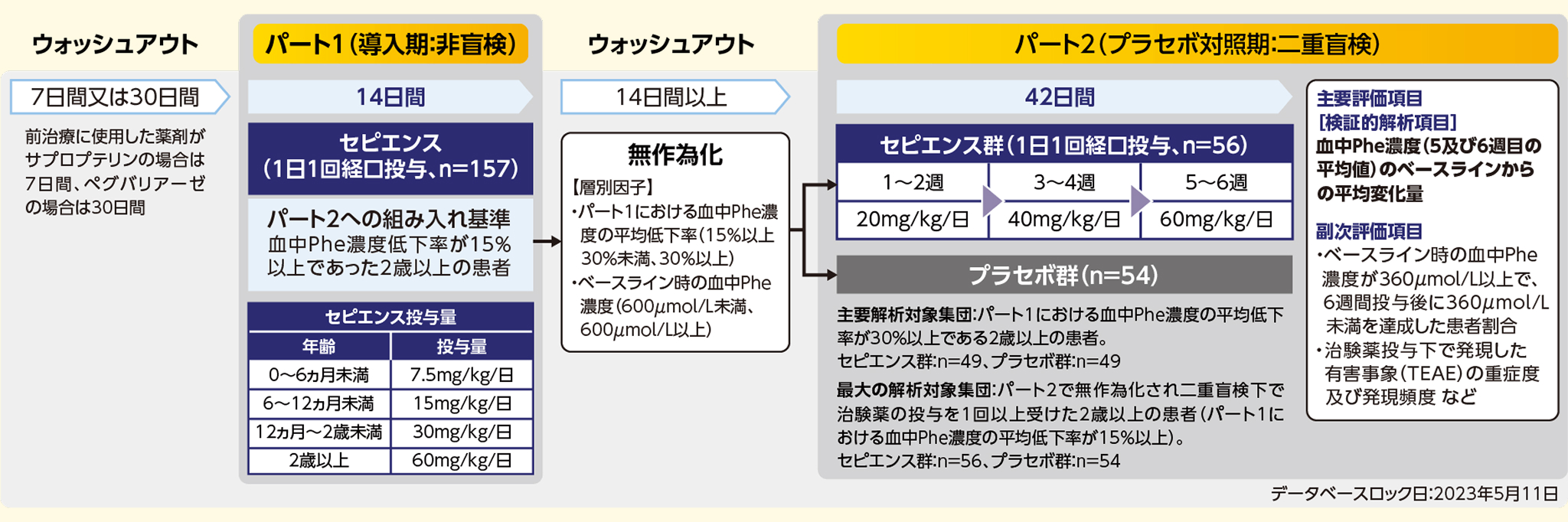
第Ⅲ相、多施設共同、2パート、無作為化、二重盲検、プラセボ対照試験。本試験はパート1(導入期:14日間、非盲検)とパート2(プラセボ対照期:6週間、二重盲検)の2パートで構成された。
主要評価項目(検証的解析項目)
副次評価項目
最大の解析対象集団は、パート2で無作為化され二重盲検下で治験薬の投与を1回以上受けた2歳以上のすべての患者とした。主要解析対象集団は、パート1における血中Phe濃度の平均低下率が30%以上である2歳以上の患者とした。安全性解析対象集団は、治験薬の投与を1回以上受けたすべての患者とした。主要解析対象集団を80例として、投与群間差を250µmol/L、投与群内標準偏差を250µmol/L、両側有意水準αを0.05と仮定した場合、主要評価項目における血中Phe濃度低下の投与群間差を検出する検出力は95%を超える。主要解析対象集団が80例となるのに必要なパート1の登録患者は約178例と算出された。古典的PKU患者*2は、試験母集団全体の20%を上限として組み入れた。
セピエンス投与により血中Phe濃度の低下率が30%以上又は15%以上30%未満の患者割合[全患者、古典的PKU患者、テトラヒドロビオプテリン(BH₄)ノンレスポンダー*3]を算出した。また、試験登録時にサプロプテリン投与中であった患者における血中Phe濃度を算出した。
主要評価項目では、血中Phe濃度(5及び6週目の平均値)のベースラインからの平均変化量について最小二乗(LS)平均値を用いて投与群間を比較し、検定は反復測定混合効果モデル(MMRM)を用いた。主要解析対象集団では、MMRMは治療、ベースライン時の血中Phe濃度、ベースライン時の血中Phe濃度区分(600µmol/L未満又は600µmol/L以上)、来院、治療と来院の交互作用を固定効果、患者を変量効果とした。最大の解析対象集団では、さらにパート1における血中Phe濃度低下区分(15%以上又は30%以上)を固定効果に追加した。副次評価項目である、ベースライン時の血中Phe濃度が600µmol/L以上で6週間投与後に600µmol/L未満を達成した患者割合、ベースライン時の血中Phe濃度が360µmol/L以上で6週間投与後に360µmol/L未満を達成した患者割合は、カイ二乗検定を用いて解析した。以上の主要評価項目及び副次評価項目における多重性の調整にはゲートキーピング法を用いた。また、各用量レベルにおける血中Phe濃度のベースラインからの平均変化量はMMRMを用いて解析した。主要評価項目では、ベースライン時の血中Phe濃度、試験登録時のサプロプテリン投与状況、BH₄反応性、古典的PKU、年齢、性別によるサブグループ解析を実施した。TEAEは、MedDRA version 26.0を用いて分類し、発現患者数(%)を要約した。
データベースロック日:
PTCC084
JP-SEP-0268
2026年3月作成
 医療関係者の方
医療関係者の方