有効性
(APHENITY試験パート1)
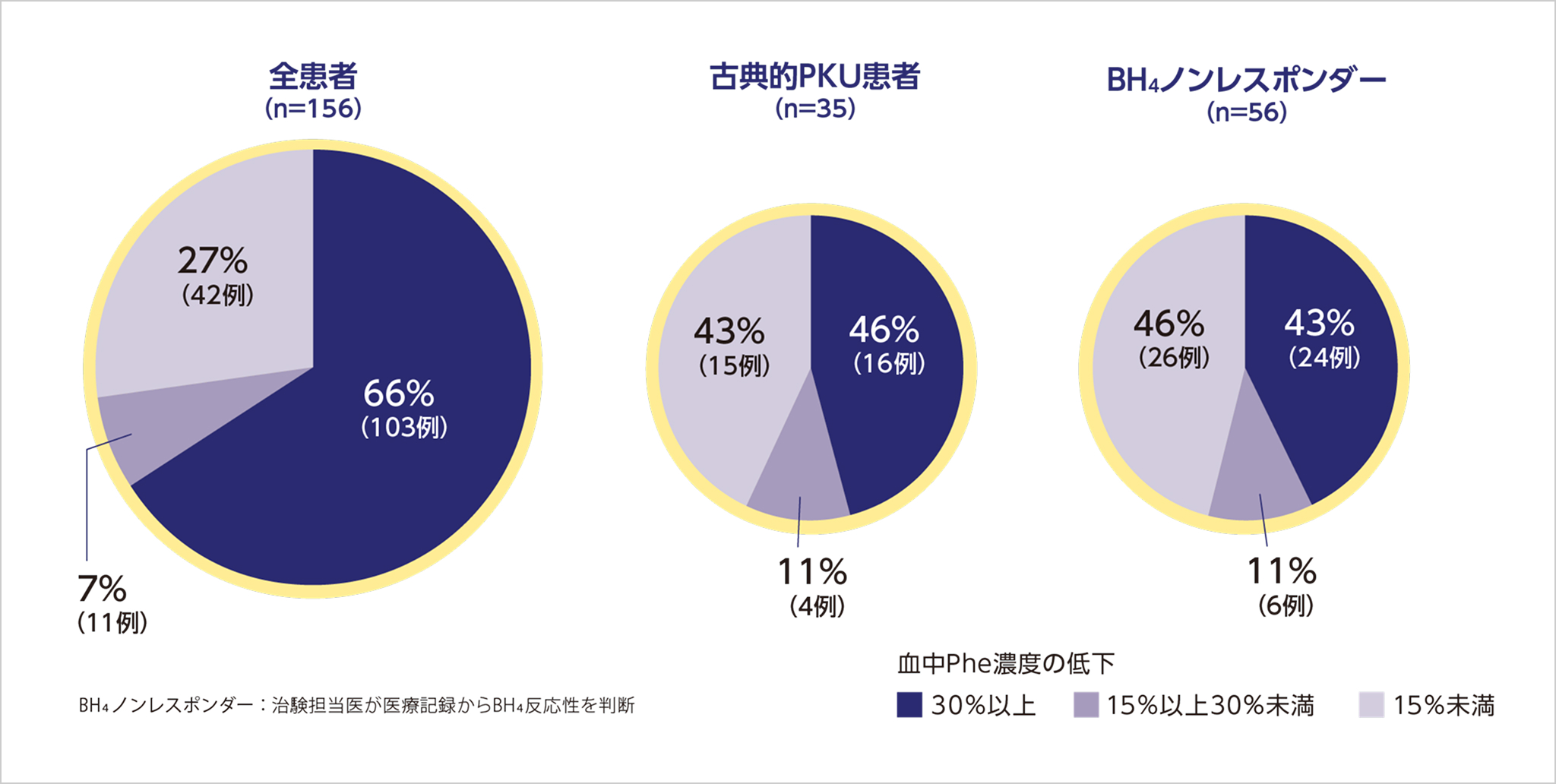
セピエンス投与により血中Phe濃度が低下した患者割合
セピエンス14日間投与により、66%の患者で血中Phe濃度が30%以上低下しました。
当サイトはセピエンスを適正にご使用いただくための情報を提供しております。
セピエンス投与により血中Phe濃度が低下した患者割合
セピエンス14日間投与により、66%の患者で血中Phe濃度が30%以上低下しました。

血中Phe濃度(5及び6週目の平均値)のベースラインからの平均変化量
プラセボ群と比べてセピエンス群で血中Phe濃度のベースライン*1からの平均変化量が有意に大きく、セピエンス群の優越性が検証されました(p<0.0001、MMRM)(検証的解析結果)。
主要解析対象集団*2
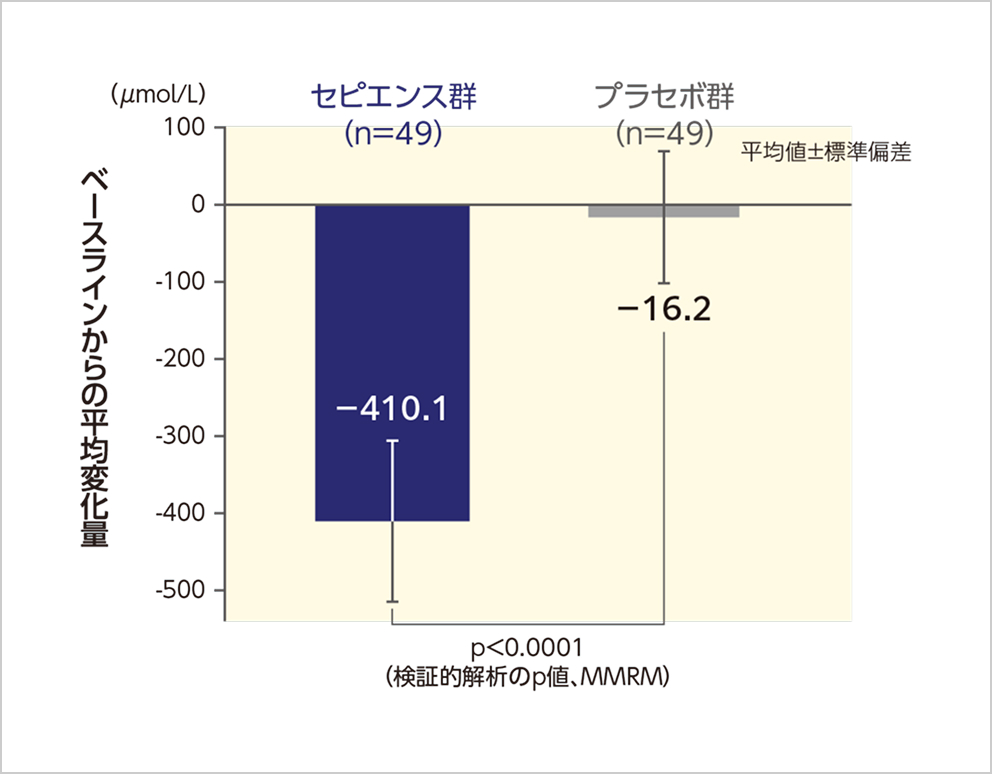
【ベースライン時の血中Phe濃度(µmol/L、平均値±標準偏差)】
主要解析対象集団
セピエンス群 : 646.1±253.0、プラセボ群 : 654.0±261.5
最大の解析対象集団
セピエンス群 : 645.6±246.1、プラセボ群 : 667.8±264.6
最大の解析対象集団*3
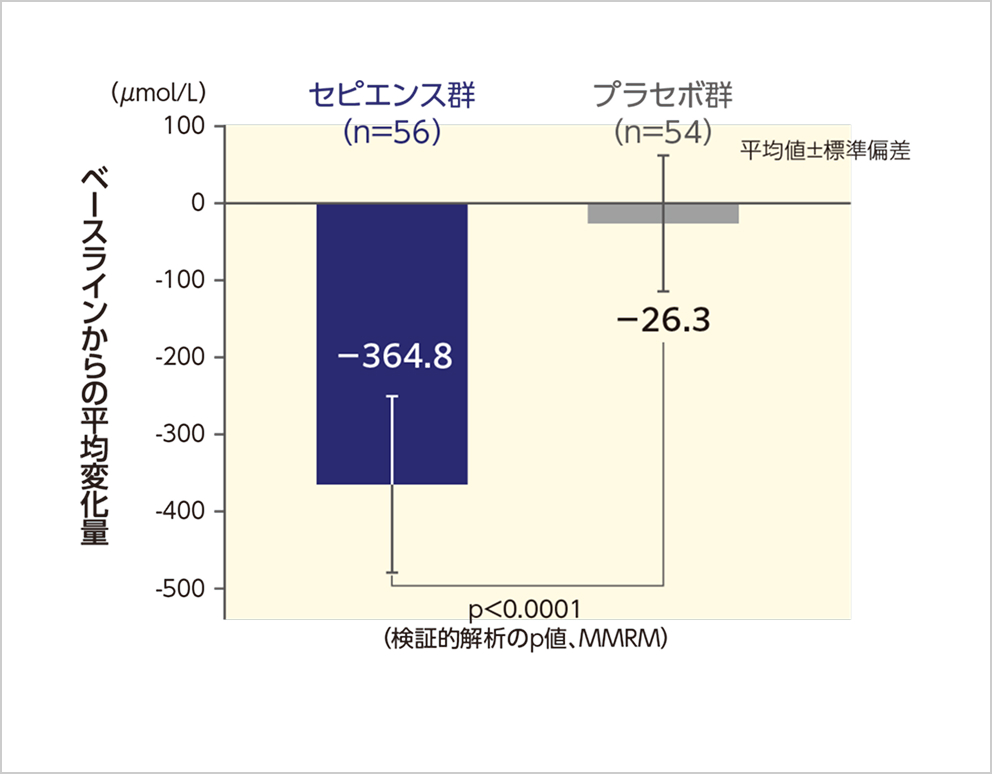
【ベースラインからの平均変化量のLS平均値(µmol/L、平均値±標準誤差)】
主要解析対象集団
セピエンス群 : -415.8±24.1、プラセボ群 : -19.9±24.2、群間差-395.9±33.8
最大の解析対象集団
セピエンス群 : -289.6±31.5、プラセボ群 : 65.3±33.0、群間差-354.9±36.4
MMRM:
反復測定混合効果モデル[主要解析対象集団の検定では、治療、ベースライン時の血中Phe濃度、ベースライン時の血中Phe濃度区分(600µmol/L未満又は600µmol/L以上)、来院、治療と来院の交互作用を固定効果、患者を変量効果とし、最大の解析対象集団の検定では固定効果にパート1における血中Phe濃度低下区分(15%以上又は30%以上)を追加した]
血中Phe濃度(5及び6週目の平均値)のベースライン*1からの平均変化量
古典的PKU患者において、セピエンス群は血中Phe濃度を低下させました。
主要解析対象集団
| ベースラインからの 平均変化量(µmol/L) |
セピエンス群 (n=6) |
プラセボ群 (n=9) |
群間差 | MMRM (名目上のp値) |
|---|---|---|---|---|
| 平均値±標準偏差 | -523.5±212.0 | -42.1±203.7 | - | - |
| LS平均値±標準誤差 | -488.2±50.5 | 4.0±46.5 | -492.2±55.6 | <0.0001 |
| [95%CI] | [-597.3~-379.1] | [-95.7~103.7] | [-614.6~-369.9] |
【ベースライン時の血中Phe濃度(µmol/L、平均値±標準偏差)】
セピエンス群:761.3±323.8、プラセボ群:771.6±283.7
MMRM:
反復測定混合効果モデル[治療、ベースライン時の血中Phe濃度、ベースライン時の血中Phe濃度区分(600µmol/L未満又は600µmol/L以上)、来院、治療と来院の交互作用を固定効果、患者を変量効果とした]
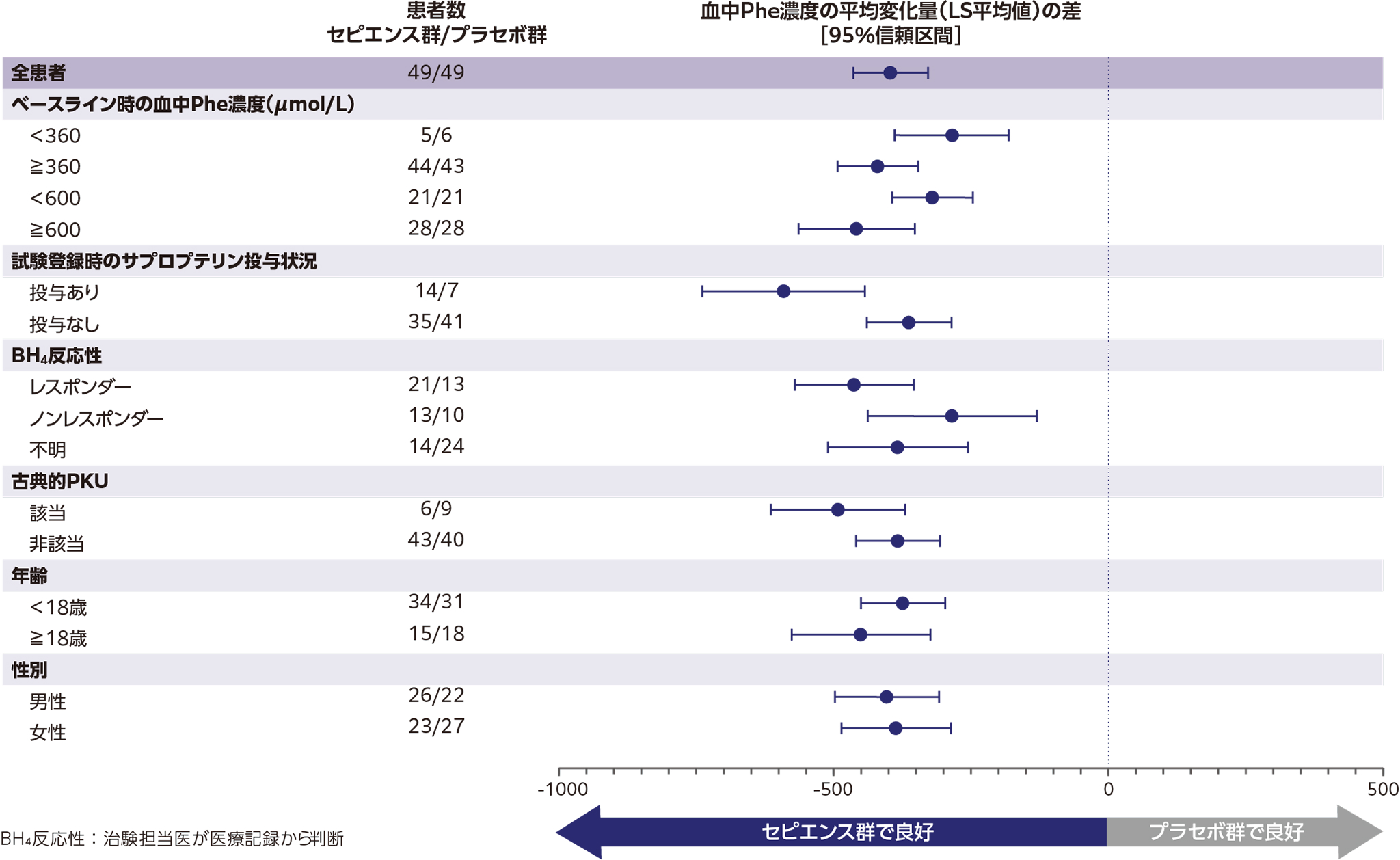
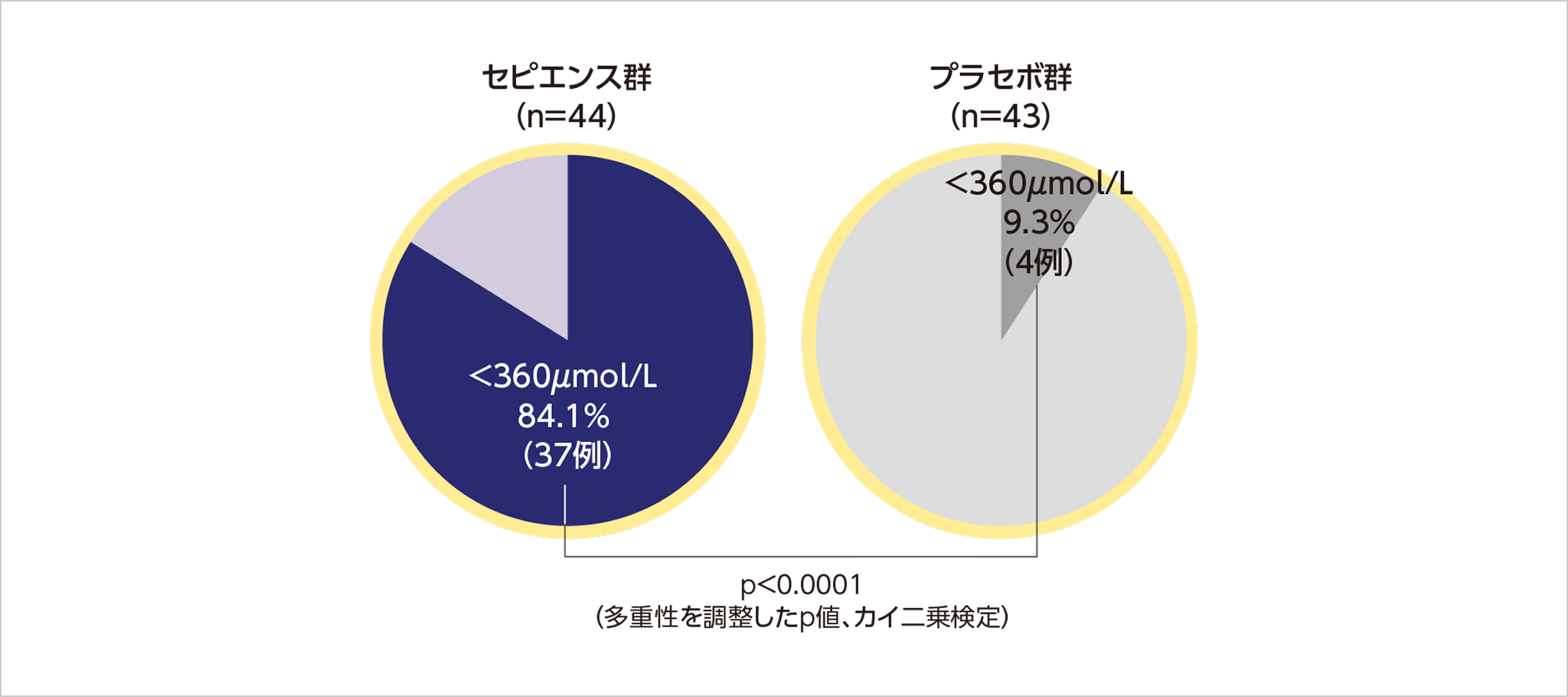
ベースライン*1時の血中Phe濃度が360µmol/L以上で6週間投与後に360µmol/L未満を達成した患者割合
血中Phe濃度が360µmol/L未満に低下した患者割合は、セピエンス群の主要解析対象集団で84.1%でした。
TEAEの重症度及び発現頻度(安全性解析対象集団)
TEAE:治験薬投与下で発現した有害事象
セピエンス群の主なTEAEは、下痢、頭痛、胃腸炎、上気道感染でした。
全体(n=157)のうち、主なTEAE(全体で5%以上に発現)は下痢8例(5.1%)、投与中止に至ったTEAEは嘔吐1例(0.6%)でした。重篤、グレード3以上、死亡に至ったTEAEは認められませんでした。
重篤、グレード3以上、投与中止、死亡に至ったTEAEは、いずれの群においても認められませんでした。
| n(%) | セピエンス群 | プラセボ群 (n=54) |
|||
|---|---|---|---|---|---|
| 20mg/kg/日 (n=56) |
40mg/kg/日 (n=56) |
60mg/kg/日 (n=55) |
全体 (n=56) |
||
| すべてのTEAE | 20(35.7) | 7(12.5) | 15(27.3) | 33(58.9) | 18(33.3) |
| 治験薬と関連のあるTEAE | 5(8.9) | 1(1.8) | 1(1.8) | 6(10.7) | 6(11.1) |
| 主なTEAE(いずれかの群で5%以上に発現)*4 | |||||
| 下痢 | 1(1.8) | 1(1.8) | 2(3.6) | 4(7.1) | 1(1.9) |
| 頭痛 | 2(3.6) | 1(1.8) | 1(1.8) | 4(7.1) | 1(1.9) |
| 胃腸炎 | 1(1.8) | 1(1.8) | 2(3.6) | 3(5.4) | 3(5.6) |
| 上気道感染 | 1(1.8) | 0 | 2(3.6) | 3(5.4) | 1(1.9) |
| 嘔吐 | 0 | 1(1.8) | 0 | 1(1.8) | 3(5.6) |
| 上咽頭炎 | 0 | 0 | 0 | 0 | 4(7.4) |
| 悪心 | 0 | 0 | 0 | 0 | 3(5.6) |
MedDRA ver26.0
PTCC084
JP-SEP-0268
2026年3月作成
 医療関係者の方
医療関係者の方