目的
フェニルケトン尿症(PKU)患者を対象に、セピエンスを経口投与したときの有効性と長期安全性を評価する。
方法
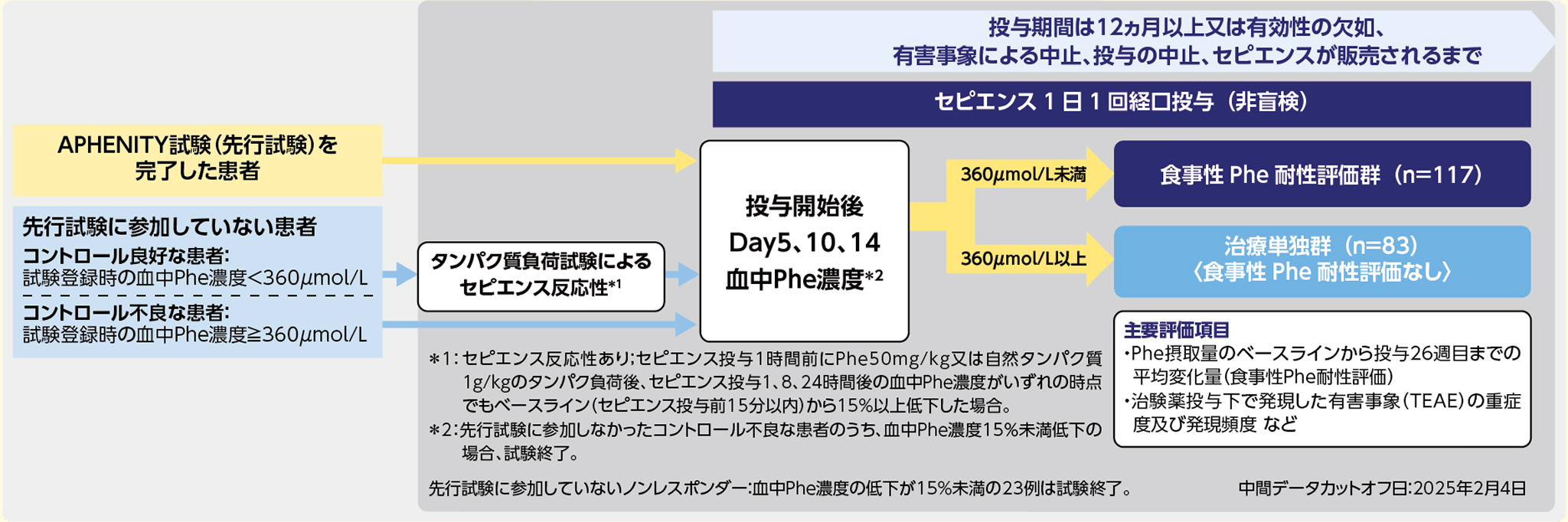
第Ⅲ相、多施設共同、非盲検試験。投与期間は少なくとも12ヵ月間又は有効性の欠如、有害事象による中止、投与中止もしくはセピエンスが販売されるまでとし、セピエンスを1日1回経口投与した。投与量は年齢に基づき、7.5mg/kg/日(生後0~6ヵ月未満)、15mg/kg/日(生後6~12ヵ月未満)、30mg/kg/日(生後12ヵ月~2歳未満)、60mg/kg/日(2歳以上)とした。
タンパク質負荷試験:7日間のタンパク質負荷(乳幼児は3日間)の後、本剤を投与し、1、8、24時間後に反応性を評価
食事性Phe耐性評価におけるPhe摂取量の調整は、下表のアルゴリズムに従い、26週間にわたって2週間間隔で実施した。
食事性Phe耐性評価におけるPhe摂取量の調整アルゴリズム2)
解析計画
最大の解析対象集団は治験薬を1回以上投与し、有効性評価を1回以上実施したすべての患者とした。
食事性Phe耐性解析対象集団は、Day5、10、14の血中Phe濃度の平均値が360µmol/L未満であり、食事性Phe耐性評価期間中に治験薬の投与を1回以上受けた患者とした。安全性解析対象集団は、治験薬の投与を1回以上受けたすべての患者とした。本試験では、セピエンスの長期安全性を評価するため、約200例の患者を登録することを計画した。
主要評価項目であるPhe摂取量のベースラインから投与26週目までの平均変化量は、中間解析では1日の食事性Phe摂取量(mg/kg/日)を要約し、ベースライン時のPhe摂取量及び週を固定効果、患者を変量効果とした反復測定混合効果モデル(MMRM)に当てはめ、最小二乗(LS)平均値を算出した。日本人サブグループに関しても、同様に解析した。
先行試験に参加していない患者について、ベースラインから投与2週目(Day5、10、14の平均値)までの血中Phe濃度の平均変化量を記述的に要約した。TEAEは、MedDRA version 26.0を用いて分類し、発現患者数(%)を要約した。