有効性
主要評価項目
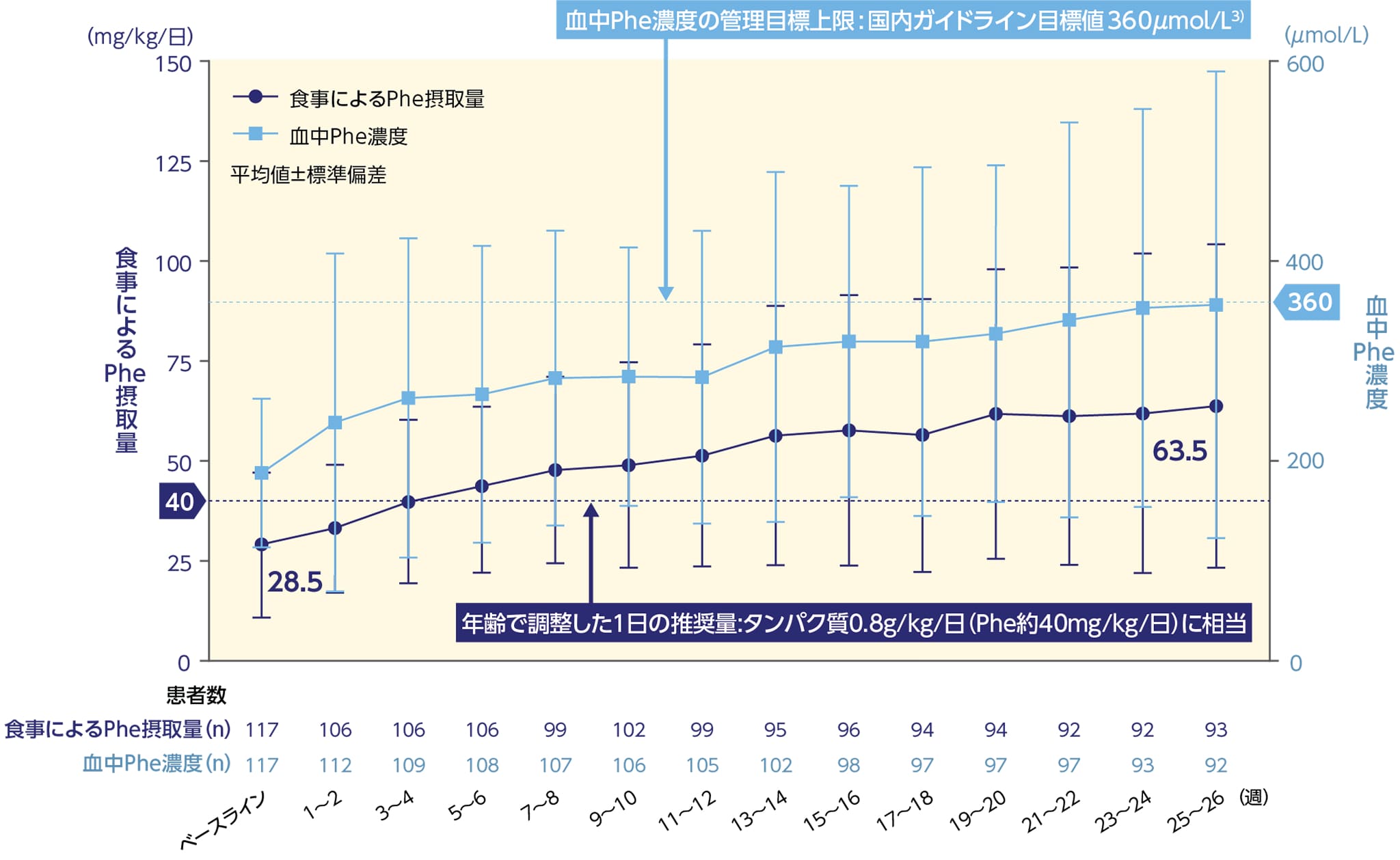
Phe摂取量のベースライン*1から投与26週目までの平均変化量(食事性Phe耐性評価)*2
血中Phe濃度が360µmol/L未満に維持された患者集団において、食事性Phe摂取量の平均値が増加しました。
食事性Phe耐性解析対象集団*3
当サイトはセピエンスを適正にご使用いただくための情報を提供しております。
Phe摂取量のベースライン*1から投与26週目までの平均変化量(食事性Phe耐性評価)*2
血中Phe濃度が360µmol/L未満に維持された患者集団において、食事性Phe摂取量の平均値が増加しました。
食事性Phe耐性解析対象集団*3

TEAEの重症度及び発現頻度(安全性解析対象集団)
TEAE:治験薬投与下で発現した有害事象
主なTEAEは、上気道感染、上咽頭炎、頭痛、下痢、嘔吐、発熱でした。
重篤なTEAEは、15mg/kg/日投与で臍ヘルニア1例(20.0%)、60mg/kg/日投与で腹痛、喘息クリーゼ、急性膵炎、喘息、出血性消化性潰瘍、鎖骨骨折が各1例(0.5%)でした。
投与中止に至ったTEAEは、60mg/kg/日投与で便秘、悪心、出血性素因、頭痛が各1例(0.5%)でした。死亡に至ったTEAEは認められませんでした。
安全性解析対象集団
| n(%) | セピエンスの用量*4 | 全体 (n=223) |
日本人 (n=15) |
|||
|---|---|---|---|---|---|---|
| 7.5mg/kg/日 (n=7) |
15mg/kg/日 (n=5) |
30mg/kg/日 (n=30) |
60mg/kg/日 (n=197) |
|||
| すべてのTEAE | 3(42.9) | 4(80.0) | 20(66.7) | 136(69.0) | 154(69.1) | 11(73.3) |
| 治験薬と関連のあるTEAE | 0 | 2(40.0) | 11(36.7) | 49(24.9) | 60(26.9) | 9(60.0) |
| 重篤なTEAE | 0 | 1(20.0) | 0 | 3(1.5) | 4(1.8) | 0 |
| CTCAEグレード3以上のTEAE | 0 | 1(20.0) | 0 | 8(4.1) | 9(4.0) | 0 |
| 投与中止に至ったTEAE | 0 | 0 | 0 | 3(1.5) | 3(1.3) | 0 |
| 主なTEAE(全体で5%以上に発現)*5 | ||||||
| 上気道感染 | 0 | 1(20.0) | 6(20.0) | 40(20.3) | 45(20.2) | 0 |
| 上咽頭炎 | 0 | 0 | 3(10.0) | 31(15.7) | 34(15.2) | 4(26.7) |
| 頭痛 | 0 | 0 | 1(3.3) | 40(20.3) | 33(14.8) | 1(6.7) |
| 下痢 | 0 | 0 | 3(10.0) | 27(13.7) | 30(13.5) | 4(26.7) |
| 嘔吐 | 0 | 1(20.0) | 6(20.0) | 20(10.2) | 26(11.7) | 3(20.0) |
| 発熱 | 2(28.6) | 0 | 4(13.3) | 20(10.2) | 24(10.8) | 0 |
| インフルエンザ | 0 | 1(20.0) | 0 | 20(10.2) | 21(9.4) | 3(20.0) |
| 咳嗽 | 0 | 0 | 1(3.3) | 20(10.2) | 21(9.4) | 0 |
| 変色便 | 0 | 1(20.0) | 8(26.7) | 7(3.6) | 16(7.2) | 4(26.7) |
| 胃腸炎 | 1(14.3) | 1(20.0) | 1(3.3) | 12(6.1) | 15(6.7) | 1(6.7) |
| 口腔咽頭痛 | 0 | 0 | 0 | 13(6.6) | 13(5.8) | 0 |
| COVID-19 | 0 | 1(20.0) | 0 | 11(5.6) | 12(5.4) | 2(13.3) |
〈CTCAEグレード3以上のTEAE〉15㎎/kg/日投与:臍ヘルニア(1例1件)、60㎎/kg/日投与:子宮内膜症、不安(1例2件)、急性膵炎、喘息、喘息クリーゼ(1例3件)、肝挫傷、胃腸炎、出血性素因、関節損傷、出血性消化性潰瘍、出血性卵巣嚢胞(各1例1件)
PTCC084
JP-SEP-0268
2026年3月作成
 医療関係者の方
医療関係者の方